Organisation européenne de vérification des médicaments (EMVO)
L´European Medicines (Verification Organisation) (EMVO), en français Organisation européenne pour l´évaluation des médicaments, a été fondée en 2015 et siège à Bruxelles. Cette création a été motivée par l´introduction de la directive 2011/62/UE (Directive sur les médicaments falsifiés (FMD)) et le règlement délégué (UE/2016/161). L´EMVO crée le système européen de vérification des médicaments (EMVS). Il vise à protéger les patients contre les médicaments falsifiés et concerne les fabricants,Grossiste en produits pharmaceutiqueset les distributeurs (pharmacies/hôpitaux).
L´EMVO se compose de plusieurs membres fondateurs. Les membres fondateurs sont
EFPIA (the European Federation of Pharmaceutical Industries and Associations - la Fédération européenne des industries et associations pharmaceutiques),
Medicines for Europe (the European Generic and Biosimilar MedicinesAssociation - l´association européenne des médicaments génériques et biosimilaires),
PGEU (the Pharmaceutical Group of the European Union, groupement des pharmaciens),
GIRP (the European Healthcare Distribution Association, association pour la distribution dans le secteur de la santé)
EAEPC (the European Association of Euro-Pharmaceutical Companies, Association européenne des entreprises pharmaceutiques)
HOPE (European Hospital and Healthcare Federation, Fédération européenne des hôpitaux et des soins de santé)
EAHP (European Association of Hospital Pharmacists, Association européenne des pharmaciens hospitaliers)
Les membres ont différentes tâches financières au sein de l´EMVO. Les contributions des grossistes et des pharmacies sont utilisées pour financer l´EMVO et le système national. Les fabricants de médicaments sont responsables du financement du développement technique de laEMVS responsable. Aucun financement public n´est nécessaire pour assurer la sécurité de la chaîne pharmaceutique.
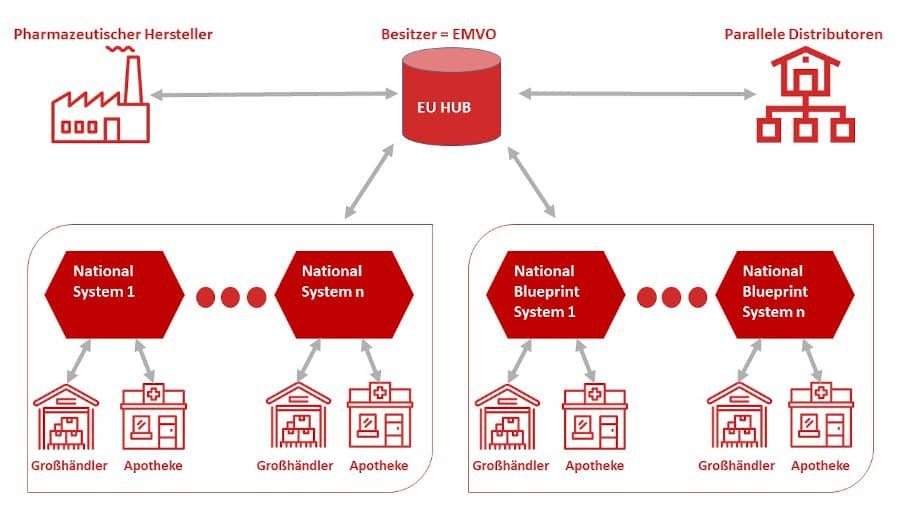
L´EMVO est le propriétaire du Hub de l´UEs. LeHub de l´UE est le point de convergence de tous les mouvements de médicaments. Toutes les informations sont enregistrées dans la base de données.
Matériel d´information sur la directive européenne MDR / IVDR
Les règlements européens entraînent de nombreuses obligations et modifications pour tous les acteurs économiques. Pour que vous sachiez tout sur vos droits et obligations, COSYS a préparé pour vous de nombreux documents d´information. C´est avec plaisir que nous mettons nos informations à votre disposition !
